经常听到有人说,生物学研究就是一个玄学,有些实验结果每次重复都不一样,我做的和他做的也不一样,干实验结果和湿实验结果也不一样!这确实是一个不争的事实,但是其实这些不一样很多情况下都是可以找到原因解释的。这些原因要么是理论上就会存在这种情况,要么就是你的某些实验条件存在差异,而你的研究对象对这些条件的反应是较剧烈的。你大可不必要求你的基因既促进肿瘤细胞活力,又促进迁移,还可以抗凋亡,总之具有全面的牛逼的抗癌能力!反之,如果有这些结果,你其实更应该高兴,因为这些问题恰恰是值得你研究的一个点,一个具有创新性的亮点!把这些看似矛盾的结果通过多次重复实验确定下来后,找到潜在的原因,再加上一些实验论证,结果起码是一篇5分以上的正经SCI论文。今天看到的这篇文章就是一个很好的例子,这或许就是科研本该有的样子吧!请看下面的摘要。
Neutrophils drive vascular occlusion, tumour necrosis and metastasis
肿瘤坏死与癌症预后不良相关,一般认为这是肿瘤生长超过营养供应时发生的被动现象。然而本研究发现,中性粒细胞会主动诱导肿瘤坏死。在多种小鼠癌症模型中,我们发现肿瘤可诱发Ly6G(High)Ly6C(Low)中性粒细胞群,这类细胞无法响应炎症刺激发生血管外渗,但比经典Ly6G(High)Ly6C(High)中性粒细胞能更高效形成中性粒细胞胞外陷阱(NETs)。这类"血管受限"中性粒细胞的存在与小鼠模型中"多形性"坏死结构的出现具有相关性。在具有多形性坏死的肿瘤中,我们发现了血管内中性粒细胞与NETs的聚集物,这些聚集物会阻塞肿瘤血管,导致下游血管床缺氧坏死。进一步研究发现,邻近坏死区域(即"坏死周边"区域)的癌细胞会发生上皮-间质转化,这解释了肿瘤坏死促进转移的矛盾现象。通过基因或药物手段阻断NET形成后,肿瘤坏死程度和肺转移均有所减少。因此,本研究通过证明NETs会驱动血管阻塞、多形性坏死和转移,表明肿瘤坏死不一定是肿瘤生长的被动副产品,且可通过阻断该过程来减少转移扩散。
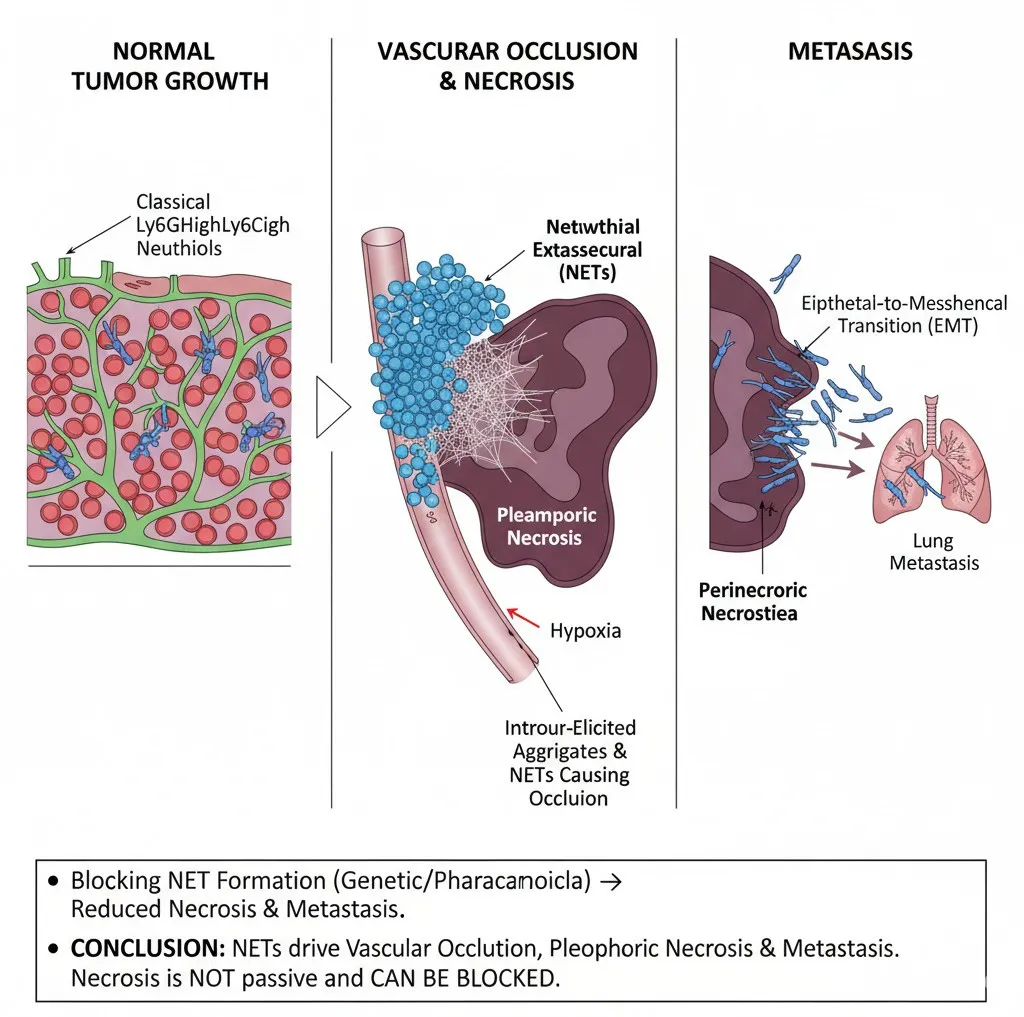
▲Graphical Abstract (由Nano Banana生成,国内版本https://sci.justscience.cn/chatgpt)
Neutrophils drive vascular occlusion, tumour necrosis and metastasis
Abstract
Tumour necrosis is associated with poor prognosis in cancer and is thought to occur passively when tumour growth outpaces nutrient supply. Here we report, however, that neutrophils actively induce tumour necrosis. In multiple cancer mouse models, we found a tumour-elicited Ly6GHighLy6CLow neutrophil population that was unable to extravasate in response to inflammatory challenges but formed neutrophil extracellular traps (NETs) more efficiently than classical Ly6GHighLy6CHigh neutrophils. The presence of these ‘vascular-restricted’ neutrophils correlated with the appearance of a ‘pleomorphic’ necrotic architecture in mice. In tumours with pleomorphic necrosis, we found intravascular aggregates of neutrophils and NETs that caused occlusion of the tumour vasculature, driving hypoxia and necrosis of downstream vascular beds. Furthermore, we found that cancer cells adjacent to these necrotic regions (that is, in ‘perinecrotic’ areas) underwent epithelial-to-mesenchymal transition, explaining the paradoxical metastasis-enhancing effect of tumour necrosis. Blocking NET formation genetically or pharmacologically reduced the extent of tumour necrosis and lung metastasis. Thus, by showing that NETs drive vascular occlusion, pleomorphic necrosis and metastasis, we demonstrate that tumour necrosis is not necessarily a passive byproduct of tumour growth and that it can be blocked to reduce metastatic spread.
这个研究的结果和我们目前实验所做的结果是非常相似的:我们的结果也是NETs对细胞活性的促进作用不明显,甚至是抑制肿瘤,但是它的促侵袭能力是非常强的。